Les bateries de liti tenen els avantatges de la portabilitat i la càrrega ràpida, així que per què continuen circulant al mercat les bateries de plom-àcid i altres bateries secundàries?
A més dels problemes de cost i dels diferents camps d'aplicació, un altre motiu és la seguretat.
El liti és el metall més actiu del món.Com que les seves característiques químiques són massa actives, quan el metall de liti s'exposa a l'aire, tindrà una forta reacció d'oxidació amb l'oxigen, de manera que és propens a explosions, combustió i altres fenòmens.A més, la reacció redox també es produirà dins de la bateria de liti durant la càrrega i la descàrrega.L'explosió i la combustió espontània són causades principalment per l'acumulació, la difusió i l'alliberament de la bateria de liti després de l'escalfament.En resum, les bateries de liti generaran molta calor durant el procés de càrrega i descàrrega, cosa que provocarà un augment de la temperatura interna de la bateria i la temperatura desigual entre les bateries individuals, provocant així el rendiment inestable de la bateria.
Els comportaments insegurs de la bateria d'ió de liti tèrmica (incloses la sobrecàrrega i la sobredescàrrega de la bateria, la càrrega i descàrrega ràpides, el curtcircuit, les condicions d'abús mecànic, el xoc tèrmic d'alta temperatura, etc.) poden provocar reaccions secundaries perilloses dins de la bateria i generar calor, danyant directament la pel·lícula passiva de l'elèctrode negatiu i la superfície de l'elèctrode positiu.
Hi ha moltes raons per desencadenar accidents tèrmics de desbordament de bateries d'ions de liti.Segons les característiques de l'activació, es pot dividir en activació d'abús mecànic, activació d'abús elèctric i activació d'abús tèrmic.Abús mecànic: es refereix a l'acupuntura, l'extrusió i l'impacte d'objectes pesats causats per la col·lisió de vehicles;Abús elèctric: generalment causat per una gestió incorrecta de la tensió o una fallada dels components elèctrics, incloent curtcircuit, sobrecàrrega i sobredescàrrega;Abús de calor: causat per un sobreescalfament causat per una gestió inadequada de la temperatura.
Aquests tres mètodes d'activació estan interrelacionats.L'abús mecànic generalment provocarà deformació o ruptura del diafragma de la bateria, donant lloc a un contacte directe entre els pols positius i negatius de la bateria i un curtcircuit, donant lloc a un abús elèctric;Tanmateix, en condicions d'abús d'electricitat, la generació de calor, com ara la calor de Joule, augmenta, fent que la temperatura de la bateria augmenti, que es converteix en un abús de calor, desencadenant encara més la reacció lateral de generació de calor de tipus cadena dins de la bateria i, finalment, conduint a l'ocurrència. fuga de calor de la bateria.
La fuga tèrmica de la bateria és causada pel fet que la taxa de generació de calor de la bateria és molt superior a la taxa de dissipació de calor i la calor s'acumula en gran quantitat però no es dissipa en el temps.En essència, la "fuga tèrmica" és un procés de cicle de retroalimentació d'energia positiva: l'augment de la temperatura farà que el sistema s'escalfi i la temperatura augmentarà després que el sistema s'escalfi, cosa que al seu torn farà que el sistema s'escalfi.
El procés de fugida tèrmica: quan augmenta la temperatura interna de la bateria, la pel·lícula SEI a la superfície de la pel·lícula SEI es descompon a alta temperatura, l'ió de liti incrustat al grafit reaccionarà amb l'electròlit i l'aglutinant, augmentant encara més la temperatura de la bateria. a 150 ℃, i es produirà una nova reacció exotèrmica violenta a aquesta temperatura.Quan la temperatura de la bateria supera els 200 ℃, el material del càtode es descompon, alliberant una gran quantitat de calor i gas, i la bateria comença a augmentar i s'escalfa contínuament.L'ànode incrustat de liti va començar a reaccionar amb l'electròlit a 250-350 ℃.El material del càtode carregat comença a experimentar una reacció de descomposició violenta i l'electròlit experimenta una reacció d'oxidació violenta, alliberant una gran quantitat de calor, generant alta temperatura i una gran quantitat de gas, provocant combustió i explosió de la bateria.
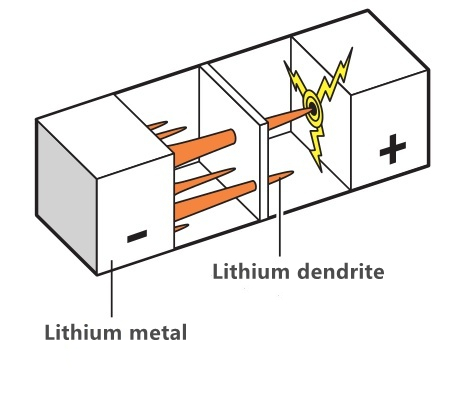
El problema de la precipitació de la dendrita de liti durant la sobrecàrrega: després que la bateria de cobalat de liti estigui completament carregada, una gran quantitat d'ions de liti queden a l'elèctrode positiu.És a dir, el càtode no pot contenir més ions de liti units al càtode, però en estat de sobrecàrrega, l'excés d'ions de liti del càtode encara nedarà cap al càtode.Com que no es poden contenir completament, es formarà liti metàl·lic al càtode.Com que aquest metall de liti és un cristall dendrític, s'anomena dendrita.Si la dendrita és massa llarga, és fàcil perforar el diafragma, provocant un curtcircuit intern.Com que el component principal de l'electròlit és el carbonat, el seu punt d'ignició i punt d'ebullició són baixos, de manera que es cremarà o fins i tot explotarà a alta temperatura.
Si es tracta d'una bateria de polímer de liti, l'electròlit és col·loïdal, que és propens a una combustió més violenta.Per resoldre aquest problema, els científics intenten substituir materials càtods més segurs.El material de la bateria de manganat de liti té certs avantatges.Pot garantir que l'ió de liti de l'elèctrode positiu es pugui incrustar completament al forat de carboni de l'elèctrode negatiu en estat de càrrega completa, en lloc de tenir certs residus a l'elèctrode positiu com el cobalat de liti, que en certa mesura evita la generació de dendrites.L'estructura estable del manganat de liti fa que el seu rendiment d'oxidació sigui molt inferior al del cobalat de liti.Fins i tot si hi ha un curtcircuit extern (en lloc d'un curtcircuit intern), bàsicament pot evitar la combustió i l'explosió causades per la precipitació del metall de liti.El fosfat de ferro de liti té una major estabilitat tèrmica i una menor capacitat d'oxidació de l'electròlit, de manera que té una alta seguretat.
L'atenuació de l'envelliment de la bateria d'ions de liti es manifesta per l'atenuació de la capacitat i l'augment de la resistència interna, i el seu mecanisme d'atenuació de l'envelliment intern inclou la pèrdua de materials actius positius i negatius i la pèrdua d'ions de liti disponibles.Quan el material del càtode està envellit i deteriorat i la capacitat del càtode és insuficient, és més probable que es produeixi el risc d'evolució de liti del càtode.Sota la condició de descàrrega excessiva, el potencial del càtode al liti augmentarà per sobre de 3 V, que és superior al potencial de dissolució del coure, provocant la dissolució del col·lector de coure.Els ions de coure dissolts precipitaran a la superfície del càtode i formaran dendrites de coure.Les dendrites de coure passaran pel diafragma, provocant un curtcircuit intern, que afecta greument el rendiment de seguretat de la bateria.
A més, la resistència a la sobrecàrrega de les bateries envellides disminuirà fins a cert punt, principalment a causa de l'augment de la resistència interna i la disminució de les substàncies actives positives i negatives, donant lloc a un augment de la calor en joule durant el procés de sobrecàrrega de les bateries.Amb menys sobrecàrrega, es poden desencadenar reaccions secundaries, provocant la fuga tèrmica de les bateries.Pel que fa a l'estabilitat tèrmica, l'evolució del liti del càtode comportarà una forta disminució de l'estabilitat tèrmica de la bateria.
En una paraula, el rendiment de seguretat de la bateria envellida es reduirà molt, cosa que posarà en perill greu la seguretat de la bateria.La solució més habitual és equipar el sistema d'emmagatzematge d'energia de la bateria amb un sistema de gestió de la bateria (BMS).Per exemple, les bateries 8000 18650 utilitzades a Tesla Model S poden realitzar un seguiment en temps real de diversos paràmetres físics de la bateria, avaluar l'estat d'ús de la bateria i realitzar un diagnòstic en línia i una alerta primerenca mitjançant el seu sistema de gestió de la bateria.Al mateix temps, també pot realitzar un control de descàrrega i precàrrega, gestió de l'equilibri de la bateria i gestió tèrmica.
Hora de publicació: desembre-02-2022